シミュレーションのリンク
扱っている現象および本教材の説明
比熱の測定は、物質固有の性質である比熱を実験的に求める熱力学の基本実験です。高温の金属球を既知の比熱を持つ水の中に入れ、熱量保存の法則を用いて金属球の比熱を計算します。
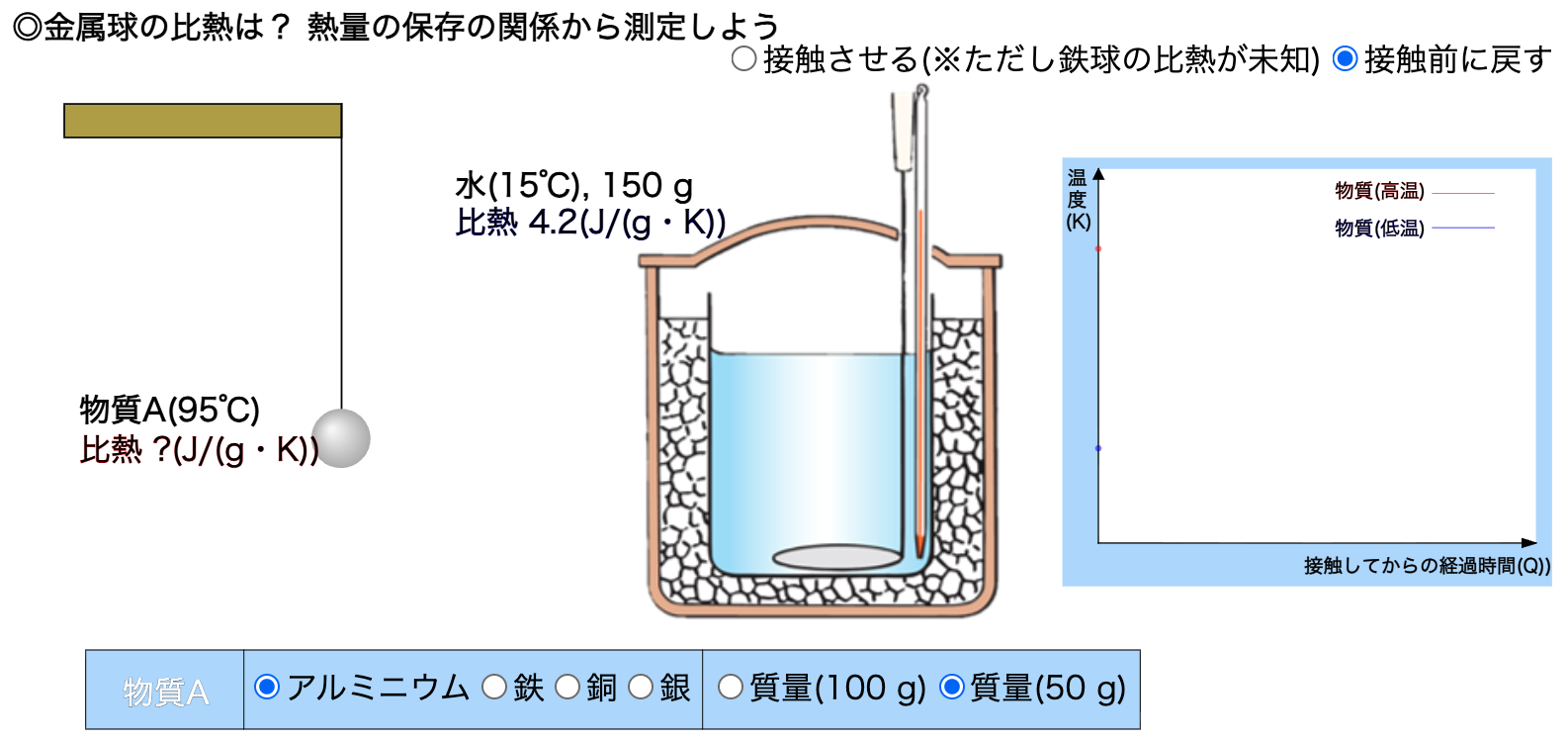
このシミュレーションでは、高温(95℃)の金属球を低温(15℃)の水の中に入れたときの温度変化を可視化し、熱平衡に達した後の温度から金属球の比熱を求めることができます。断熱容器を使用することで、外部への熱損失を防ぎ、熱量保存の法則が成り立つ条件を実現しています。
比熱とは
比熱とは、物質1gの温度を1K(または1℃)上昇させるのに必要な熱量のことです。物質によって比熱は異なり、物質を特定する重要な物性値の一つです。
主な物質の比熱:
- 水: 4.2 J/(g·K)
- アルミニウム: 0.90 J/(g·K)
- 鉄: 0.45 J/(g·K)
- 銅: 0.38 J/(g·K)
- 銀: 0.24 J/(g·K)
熱量保存の法則による比熱の測定原理
断熱容器の中で高温の金属球と低温の水が熱平衡に達するとき、以下の関係が成り立ちます:
金属球が失った熱量 = 水が得た熱量
m金属 × c金属 × (T金属初 - T平衡) = m水 × c水 × (T平衡 - T水初)
ここで:
- m金属: 金属球の質量 [g]
- c金属: 金属球の比熱 [J/(g·K)](未知数)
- T金属初: 金属球の初期温度 [℃]
- m水: 水の質量 [g]
- c水: 水の比熱 4.2 [J/(g·K)]
- T水初: 水の初期温度 [℃]
- T平衡: 熱平衡温度 [℃]
この式を変形すると、未知の比熱c金属を求めることができます:
c金属 = (m水 × c水 × (T平衡 - T水初)) / (m金属 × (T金属初 - T平衡))
測定の条件
正確な測定のためには以下の条件が必要です:
- 断熱容器を使用し、外部との熱の出入りを防ぐ
- 十分に時間をおいて、完全に熱平衡に達する
- 温度計の精度を確保する
- 容器や温度計の熱容量を無視できる場合、または補正する
対象
- 中学校・高校で物理(熱分野、比熱)を学習している学生
- 大学初年次の熱力学実験を行う学生
- 熱量保存の法則と比熱測定の原理を視覚的に理解したい学習者
使用方法
- シミュレーションを開始すると、高温の金属球(95℃)と水(15℃、150g)が分離した状態で表示されます
- 画面下部で金属球の種類(アルミニウム、鉄、銅、銀)と質量(100g、50g)を選択します
- 「接触させる(※ただし鉄球の比熱が未知)」のラジオボタンを選択すると、金属球が水の中に入ります
- 接触後、時間経過とともに金属球と水の温度が変化する様子がグラフに表示されます
- グラフには物質(高温)と物質(低温)の2本の線が表示され、最終的に熱平衡温度に収束します
- 熱平衡温度から、熱量保存の法則を使って金属球の比熱を計算できます
- 「接触前に戻す」のラジオボタンを選択すると、初期状態に戻ります
- グラフの横軸は接触してからの経過時間[s]、縦軸は温度[K]を表しています
観察のポイント
- 金属球を水に入れると、金属球の温度は下がり、水の温度は上がることを確認しましょう
- 時間が経過すると両者の温度が近づき、最終的に同じ温度(熱平衡温度)に達することを観察しましょう
- 金属球の質量が大きいほど、水の温度上昇が大きくなることを確認しましょう
- 金属の種類によって熱平衡温度が異なることを観察しましょう(比熱が異なるため)
- 熱平衡温度から、熱量保存の法則を使って金属球の比熱を計算してみましょう
- 計算した比熱が、既知の値と一致するか確認しましょう
- 断熱容器を使用することで、熱量保存の法則が精度よく成り立つことを理解しましょう
発展的な内容
計算例
例えば、50gの鉄球(95℃)を150gの水(15℃)に入れ、熱平衡温度が20℃になったとします。鉄の比熱を求めてみましょう:
鉄球が失った熱量 = 水が得た熱量 50 × c鉄 × (95 - 20) = 150 × 4.2 × (20 - 15) 50 × c鉄 × 75 = 150 × 4.2 × 5 3750 × c鉄 = 3150 c鉄 = 3150 / 3750 = 0.84 J/(g·K)
(実際の鉄の比熱は約0.45 J/(g·Kです。この例では説明のための仮の値を使用しています)
測定誤差の要因
実際の実験では、以下の要因により誤差が生じます:
- 熱損失: 断熱が完全でないため、周囲への熱の逃げがある
- 容器の熱容量: 容器自体も熱を吸収するため、無視できない場合がある
- 温度計の熱容量: 温度計も熱を吸収する
- 測定時間: 完全に熱平衡に達する前に測定すると誤差が生じる
- かき混ぜ不足: 水の温度が均一でないと正確な測定ができない
比熱と熱容量の関係
- 比熱 (c): 単位質量あたりの温度を1K上げるのに必要な熱量 [J/(g·K)]
- 熱容量 (C): 物体全体の温度を1K上げるのに必要な熱量 [J/K]
- 関係式: C = mc
比熱は物質固有の値ですが、熱容量は質量にも依存します。